电解液锂盐是锂离子电池电解液的重要组成部分,目前市场上广泛使用的是六氟磷酸锂LiPF6-碳酸盐电解液。LiPF6具有溶解性好、离子电导率高、离子解离度高等优点。但其热稳定性差,易水解生成HF,是电池性能下降的重要原因。因此,近年来人们一直在努力寻找性能更好的新型锂盐来替代传统锂盐LiPF6。
LiFSI是最近流行的一种新型锂盐。由于其比LiPF6具有更好的热稳定性、离子导电性和更高的锂离子迁移数,Lifsi是高性能锂离子电池中最有希望取代LiPF6的锂盐。但目前LiFSI的价格远高于LiPF6,完全替代LiPF6作为电解液中主要锂盐的成本太高,难以在商业上推广。我们用LiFSI作为辅助锂盐,与LiPF6混合,充分发挥它们的优势。研究了添加锂硅对电池物理化学性能、电解液离子电导率和倍率性能的影响。
1实验
1.1 电解液的配制及参数测定
在氩气气氛的手套箱中[棕色(H2O)110-6,棕色(O2)110-6]将碳酸乙烯酯(EC)、碳酸二甲酯(DMC)、碳酸乙基甲酯(EMC)和六氟磷酸锂(LiPF6)制备成1.2 mol/l的ipf6/(EC EMC DMC),分别加入0.1/0.3/0.5mol/L的氟磺酰亚胺锂(LiFSI)制备混合盐电解液。电解液的含水量采用METTLERTOLEDODL32卡尔费休水分测定仪测试,后续实验采用达到电池级标准[(H2O)1.510-5]的电解液。
在氩气气氛的手套箱中,将装有电解液的烧杯放入温度控制在(251)的油浴锅中,用乌氏粘度计(=0.5 ~ 0.6 mm)连续测试电解液的运动粘度3次,取平均值;用DDS-307电导率仪测量电解液的电导率。
在氩气气氛的手套箱中,以金属锂为正负极,以Celgard2400膜为隔膜,加入自制电解液,组装成两端不同电解液不堵Li的电池:Li|电解液|Li电池。参考恒电位极化法,用SL1287 1260电化学工作站测量电解液的锂迁移数()。当对电池施加10mV的电压D时,初始电流I0下降到稳态电流Iss,极化前后电池电极电荷转移阻抗和钝化膜阻抗之和分别为Io和Iss。根据公式(1)计算t。
1.2 LiFePO4/Li半电池的组装与性能测试
将磷酸铁锂(磷酸铁锂)、导电剂超级炭黑super和聚偏氟乙烯(PVDF)按质量比811混合均匀,然后加入N-甲基吡咯烷酮(NMP),搅拌成均匀的浆料,涂覆在20 mm厚铝箔(99.9%)的集流体上,在120 (-0.1MPa,
在氩气气氛手套箱中,以锂金属片为负极、磷酸铁锂为正极组装了CR2025纽扣电池,并用CHI660C电化学工作站进行了循环伏安和交流阻抗测试
。循环伏安测试的电位为2.5~4.0V,扫描速率为0.1mV/s;交流阻抗测试的频率为105~10-2Hz,交流扰动电压为5mV。1.3 18650型电池的组装与性能测试
按质量比91.0:1.0:2.0:1.5:4.5将LiFePO4、超级碳黑SuperP、导电石墨KS6、碳纳米管(CNT)和PVDF混匀,然后加入NMP,搅拌成均匀的浆料,用转移式涂布机涂覆在铝箔集流体上,在120℃下真空干燥24h,再以8MPa的压力压成137滋m厚,分切成80cm×5.3cm的LiFePO4电极(含8.5g活性物质)。
按质量比93: 2:5将天然石墨(AGP)、超级碳黑SuperP和PVDF混匀,然后加入NMP,搅拌成均匀的浆料,用转移式涂布机涂覆在12滋m厚的铜箔(99.9%)集流体上,在120℃下真空干燥24h,再以11.5MPa的压力压成82滋m厚,分切成86cm×5.4cm的AGP电极(含5.0g活性物质)。
根据LiFePO4和AGP的比容量,设计正负极活性物质的质量配比及相应的电池工艺参数(负极容量约过量3%)。将制好的电极与Celgard2400膜卷绕成电芯,经装壳焊接、滚槽、85℃真空干燥24h、注液(6g)及密封等工艺,制成18650型实验电池。
用5V/10A自动充放电仪对电池进行化成,以0.5A恒流充电至3.65V,转恒压充电至0.1A,静置10min后,以0.5A恒流放电至2.30V,循环3次。用恒流限压、恒压限流的充放电制度,在5V/20A自动充放电仪上进行倍率特性测试,电压为3.65~2.00V。
2结果与讨论
2.1 电解液电导率、黏度及锂离子迁移数
电导率是体现电解液离子传导能力的一个重要物化参数,在一定程度上反应了电解质中电流的传输速度和电池内部阻抗。在一定的温度下,电解液电导率与其黏度、锂盐浓度等因素直接相关。离子迁移数反应了某种离子运载的电流与通过溶液的总电流之比。在充放电过程中,锂离子电池的电极反应所需要的电荷转移主要由Li+承担,而高的Li+迁移数能减轻电极反应的浓差极化,使电池产生高的比能量和比功率。一般来说,电导率和锂离子迁移数直接反映了电解液的导离子能力。

采用恒电位极化法测得锂离子迁移数,图1为1.2mol/LLiPF6-0.1mol/LLiFSI电解液锂离子迁移数测试结果,由电流-时间曲线图1(a)和极化前后电池阻抗谱图图1(b)组成。对电极体系加上10mV电势差,初始时浓度梯度为零,流过电池两端的电流为正负离子在电场力作用下的电迁移所决定,其初始电流为I0,随后电流下降并达到稳态,稳态时负离子的运动对电流的贡献为零,即体系的电流都是由正离子的运动所贡献的,稳态电流为Iss。当电池极化前后,电极表面电荷转移阻抗以及钝化膜阻抗发生了变化,其值对应于阻抗谱的第一个半圆直径。根据式(1)计算电解液的锂离子迁移数。
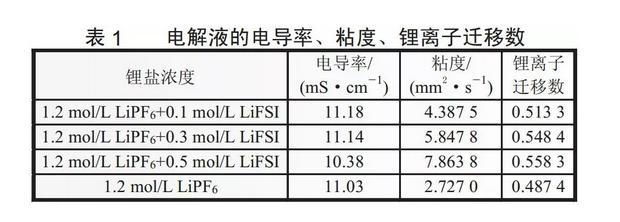
表1列出了加入不同量LiFSI后混合锂盐电解液的电导率、粘度及锂离子迁移数。从表1中数据可知,当加入0.1mol/LLiFSI时,电导率由11.03增大到了11.18,同时锂离子迁移数也由0.4874增大到0.5133;当LiFSI浓度增加到0.3mol/L时,因为粘度的增加使电导率有所下降,但仍高于未加LiFSI电解液的电导率,而此时锂离子迁移数仍在增加;当LiFSI浓度进一步增大到0.5mol/L时,电导率继续下降,低于未加LiFSI电解液,而此时锂离子迁移数仍在增加。这说明加入适量的LiFSI能够提高电解液的电导率和锂离子迁移数,增大其导离子能力。
2.2 LiFePO4/Li半电池电化学阻抗与循环伏安测试
为了分析LiFSI的加入对电解液/LiFePO4界面的影响,以LiFePO4为工作电极、Li为对电极进行了循环伏安和交流阻抗测试。
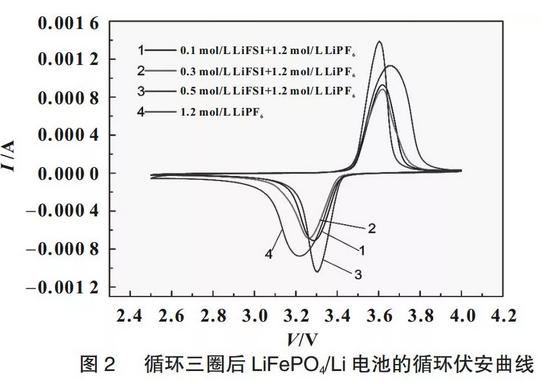
图2为使用不同电解液的LiFePO4/Li半电池充放电3次后的循环伏安谱图,由图2可知,随着LiFSI的加入,氧化峰和还原峰的峰位差在减小,说明LiFePO4的电极反应的可逆性在增加,这一方面是因为LiFSI的加入使电解液的锂离子迁移数增大,能够减小电池的浓差极化,提高电极反应的可逆性;另一方面也表明LiFSI的加入有助于在LiFePO4表面形成稳定的、导离子性好的钝化膜,这一推测在电池的电化学阻抗谱中也得到了证实。
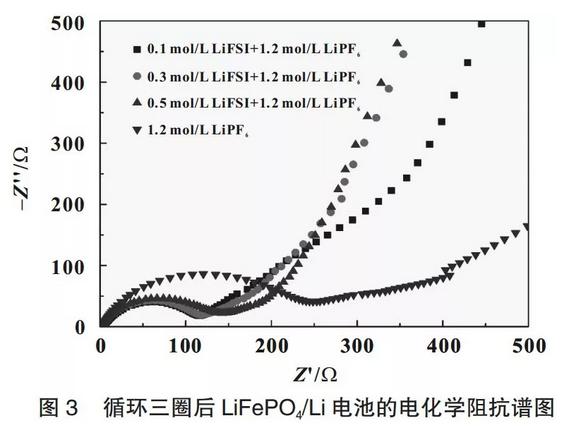
图3为循环三圈后电池的电化学阻抗,电化学阻抗谱的Nyquist曲线由高、中频区的半圆和低频区的斜线组成,高、中频区的半圆对应于工作电极表面钝化膜阻抗以及电解液/电极界面电荷转移阻抗之和,低频区的斜线为Li+在电极中的扩散阻抗[7-8]。由图3可知,相对于纯LiPF6电解液,LiFSI的加入明显降低了电解液/电极界面的阻抗,这说明LiFSI的加入使LiFePO4表面形成更有利于锂离子通过的钝化膜。
2.3 LiFePO4/石墨18650全电池倍率性能测试
为了考察混合盐电解液在高功率电池中的应用,制备了LiFePO4/石墨18650全电池,对其进行0.5~20的倍率放电,测试结果如图4所示。
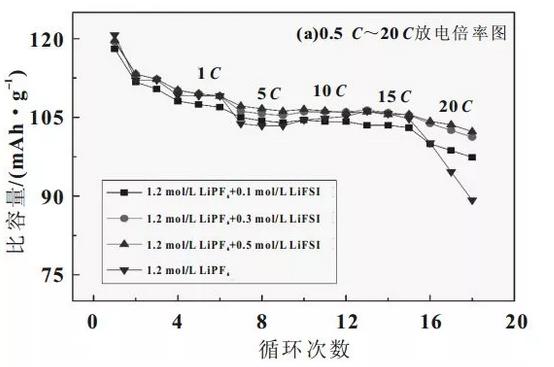
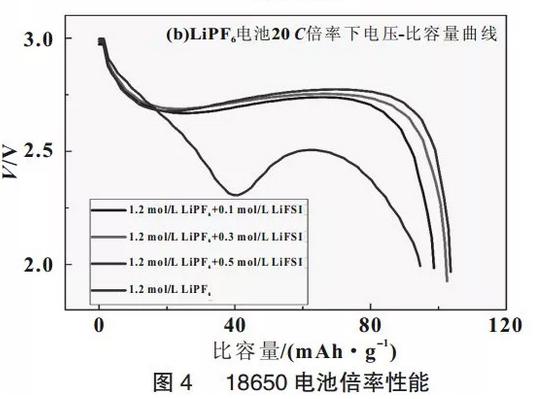
由图4(a)可知,在倍率增大到15前,放电比容量大小存在微小的差异,随着倍率继续增大到20时,放电容量开始出现较明显的不同,尤其是1.2mol/LLiPF6电解液的电池的放电性能衰减很快,由0.5的120.2mAh/g衰减到86.3mAh/g,容量保持率为71.8%;而加入0.5mol/LLiFSI的电解液电池则是从120mAh/g衰减到102.3mAh/g,容量保持率体高度了85.2%,图4(b)为20放电时的电压-容量曲线,从图4中可见,LiFSI的加入大大改善了20放电性能,平均放电电压由2.3V提高到2.75V,放电容量也有所提高。这主要源于LiFSI的加入,使得锂离子迁移数增大,电解液中可迁移的Li+数目增多,浓差极化减弱,同时在电极表面形成阻抗较低的钝化膜,这些因素使得LiFSILiPF6混合盐电解液适合于高倍率放电。
3结论
研究表明,LiFSI加入LiPF6电解液中能够提高电解液的电导率和锂离子迁移数,增强电解液导离子能力;同时LiFSI有助于降低电极表面膜阻抗,形成稳定的、导离子性较好的钝化膜;18650全电池倍率测试结果表明LiFSI-LiPF6混合盐更适用于高功率锂电池。